CLORINACION / CHLORINATION/
CLORAÇÃO
CLORINACION
Uno de los miles de los progresos humanos, es la clorinación de aguas de abastecimiento publico para prevenir la diseminación de enfermedades provenientes del agua. En la acuicultura, la clorinación también es ampliamente usada para desinfectar laboratorios de peces y camarones; y algunas veces es usada para desinfectar estanques de producción en preparación para la siembra.
Recientemente, el uso de la clorinación en la acuicultura se ha ampliado para destruir organismos
patógenos, controlar la abundancia de fitoplancton y mejorar la calidad del agua en estanques ya
sembrados con peces o camarones. Esta aplicación de la clorinación no ha sido evaluada objetivamente, pero parece que es pobremente concebida., debido a que las bajas concentraciones de cloro son tóxicas a los animales acuáticos. A pesar de esto, muchos cultivadores de peces y camarones desearían saber si la clorinación de los estanques de engorde pueden ser benéficos y la siguiente discusión de química de cloro y clorinación deberían ayudarlos a decidir.
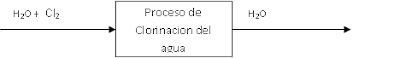
Balance de Masa:
Los compuestos comunes de cloro comercial para la desinfección son: gas clórico (Cl2),
hipoclorito de sodio (NaOCl) e hipoclorito de calcio Ca(OCl)2. El cloro reacciona con el agua para
formar un ácido fuerte (ácido hidroclorico) y un ácido débil (ácido hipocloroso o HOCl) como sigue:
Cl2 + H2O -------- HOCl H + Cl
El ácido hipocloroso se disocia para producir ion hidrógeno (H+) e ion hipoclorito (OCl ), de
acuerdo a la ecuación siguiente:
HOCl -------- H + OCL
m1 + m2 = m3
17.5lt/s + 3500gr = 17.5lt/s
Por esto, la clorinación del agua produce cuatro especies clóricas: cloro, cloruro (Cl), ácido hipocloroso e hipoclorito. El cloro, ácido hipocloroso e hipoclorito son denominados cloro residuales libres. Los poderes desinfectantes del cloro y ácido hipocloroso son aproximadamente 100 veces mayores que aquel del hipoclorito. El cloro residual libre dominante en el agua depende del pH, que en vez del tipo de compuesto de cloro aplicado.
El cloro está solo presente a pH muy bajos; el HOCl es el residual dominante entre pH 2 y 6; tanto el HOCl y OCl están presentes en porciones significativas entre pH 6 y 9; pero el HOCl declina relativo al OCl al incrementar el pH; el OCl es el residual dominante por encima de pH 9.
La desinfección a pH 7 normalmente requiere aproximadamente 1 mg/L de residuos de cloro
libres. La tasa HOCl:OCl disminuye al incrementares el pH y son requeridas concentraciones mayores de residuales de cloro libres al ir subiendo el pH debido a que la potencia de desinfección disminuye al ir disminuyendo la proporción de HOCl en los residuales de cloro libres. La Tabla 1 compara la concentración de residuales de cloro libres necesarios a diferentes valores de pH para igualar la potencia de desinfección de 1 mg/L de residuales de cloro libres a pH 7. Generalmente, el pH de los estanques de engorde está por encima de 7.5 y debido a la remoción del dióxido de carbón por el fitoplancton para el uso en la fotosíntesis, el pH por las tardes puede ser 8.5 a 9. Por lo que, dosis elevadas de cloro serán necesarias para proveer residuales de cloro libres suficientes para eliminar microorganismos. También debe ser anotado que unas cuantas horas de exposición a los residuales de cloro libres de 0.1 - 1.0 mg/L pueden causar mortalidades significativas de animales acuáticos.
En la mayoría de las aguas, las concentraciones de residuales de cloro son menores que la
dosis del agente clorinante, debido a que los residuos de cloro se pierden mientras ellas oxidan otros compuestos y cuando se combinan con la materia orgánica. La demanda de cloro es la dosis de cloro menos el residuo de cloro.
Determinación del porcentaje de remoción de los microorganismos indicadores


No hay comentarios:
Publicar un comentario